Тема 5. Окислительно-восстановительные процессы
5.1. Окислительно-восстановительные реакции.
Электронные представления об окислении и восстановлении. Химические реакции могут протекать без изменения или с изменением степени окисления элементов, например:
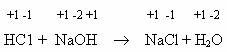
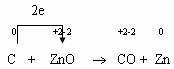
Если в первом примере (реакция нейтрализации) ни один из элементов не меняет степени окисления, то во втором - изменяется от +2 до 0 степень окисления цинка и от 0 до +2 степень окисления углерода.
Реакции, протекающие с изменением степени окисления элементов, называются окислительно-восстановительными.
Изменение степеней окисления произошло очевидно вследствие перехода двух электронов от углерода к цинку, что может быть выражено электронными уравнениями полуреакций окисления и восстановления, которые при сложении дают уравнение окислительно-восстановительной реакции:
восстановитель 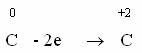 окисление;
окисление;
окислитель 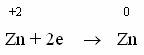 восстановление;
восстановление;
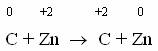
Элемент, отдающий электроны, называется восстановителем, в ходе реакции он окисляется, его степень окисления увеличивается.
Элемент, принимающий электроны, называется окислителем, в ходе реакции он восстанавливается, его степень окисления уменьшается.
Понятия окислитель и восстановитель распространяются также на простые и сложные вещества, содержащие соответствующие элементы. В приведенном примере восстановителем является простое вещество: углерод С, окислителем - сложное вещество: оксид цинка ZnO.
В общем случае окислительно-восстановительная реакция может быть обратимой, в результате восстановитель превращается в окислитель, а окислитель - в восстановитель:
восстановитель - ne ↔ окислитель
окислитель + ne ↔ восстановитель
Таким образом, окислительно-восстановительная реакция представляет собой неразрывное единство двух полуреакций - окисления и восстановления, причем количества электронов, отданных восстановителем и принятых окислителем равны.
Окислительно-восстановительные свойства простых и сложных веществ. Простые вещества - металлы, обладая небольшой электроотрицательностью, сравнительно легко теряют электроны, проявляя исключительно восстановительные свойства. Наиболее ярко они выражены у щелочных металлов. Для простых веществ - неметаллов с большой электроотрицательностью характерны окислительные свойства. Абсолютным окислителем является фтор, ярко выражены окислительные свойства также у кислорода (кроме реакции с фтором, где кислород играет роль восстановителя). Однако неметаллы со сравнительно небольшой электроотрицателъностью, например углерод, водород наряду с окислительными могут проявлять и восстановительные свойства, отдавая электроны более сильным окислителям.
Сложные вещества могут быть окислителями или восстановителями в зависимости от величины степени окисления элементов, входящих в их состав.
Если степень окисления элемента в данном соединении велика, он имеет возможность понизить ее, принимая электроны. Вещество в таком случае будет окислителем. Важнейшими окислителями являются: азотная кислота НNOз и ее соли - нитраты, тетраoксид азота N2O4, соли хлорной кислоты НС1О4- перхлораты, перманганат калия КМпО4 и др.
Если в состав соединения входит элемент с небольшой степенью окисления, он может ее повысить, отдавая электроны. Сложное вещество, содержащее такой элемент, будет проявлять восстановительные свойства. Важнейшими восстановителями являются аммиак NН3, гидразин N2H4 и его органические производные, углеводороды, спирты, амины и другие вещества.
Очевидно, если в состав соединения входит элемент с промежуточной степенью окисления, он может понизить ее, принимая электроны, или повысить, отдавая электроны. Понятия окислитель и восстановитель в этом случае становятся относительными: вещество в зависимости от свойств партнера по реакции будет проявлять либо окислительные, либо восстановительные свойства. Примером может служить пероксид водорода Н2О2, степень окисления кислорода в котором равна -1. Ее величина может уменьшиться до -2 путем присоединения одного электрона или увеличиться до 0 путем его отдачи. Поэтому при взаимодействии с энергичными восстановителями пероксид водорода ведет себя как окислитель, а в реакции с энергичными окислителями - как восстановитель.
Составление уравнений окислительно-восстановительных реакций.
Окислительно-восстановительные реакции часто выражается сложными уравнениями. Для подбора коэффициентов в них применяют два метода: метод электронных уравнений и метод электронно-ионных уравнений.
Метод электронных уравнений базируется на понятии степени окисления. Он носит универсальный характер и применим для всех типов окислительно-восстановительных реакций. Метод включает следующие операции:
1. Записывают схему реакции с указанием степени окисления элементов, например:
![]()
2. Определяют элементы, изменившие степень окисления. В данной реакции степень окисления изменили углерод и азот, у водорода и кислорода величина степени окисления осталась неизменной.
3. Составляют электронные уравнения полуреакций окисления и восстановления с соблюдением равенства масс и зарядов:
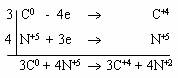
Числа электронов, отданных восстановителем и принятых окислителем должны быть равны, поэтому следует первое уравнение умножить на три, а второе - на четыре. Указанные множители являются коэффициентами для восстановителя С, окислителя HNO3 и продуктов их превращений СО и NO:
4. Коэффициенты для остальных веществ, состоящих из элементов с неизменной степенью окисления, находят из баланса соответствующих атомов в левой и правой частях уравнения. В рассмотренной реакции таким веществом является вода, перед формулой которой нужно поставить коэффициент два. Окончательное уравнение запишется в виде:
Метод электронно-ионных уравнений применяют при составлении уравнений реакций, протекающих в растворах электролитов. В этом случае степень окисления не определяется, а процессы окисления и восстановления записываются для реальных ионов и молекул, находящихся в растворе.
С целью сохранения баланса масс используют частицы среды, в которой протекает реакция. В любых водных растворах это молекулы воды, в кислых - дополнительно ионы Н + и в щелочных - ионы ОН-.
Последовательность действий следующая:
1. Составляют ионную схему реакции, записывая сильные электролиты в виде ионов, газообразные, нерастворимые вещества и слабые электролиты в виде молекул:
С + Н+ + NO3- ® CO2 + NO + Н2О
2. 3аписывают электронно-ионные уравнения полуреакций окисления и восстановления.
В данной реакции в роли восстановителя выступает углерод С, который окисляясь превращается в диоксид углерода СО2. Для сохранения баланса масс в левую часть уравнения добавляют две молекулы Н2О, а в правую - четыре иона Н-. Баланс зарядов сохраняют, отнимая от левой части уравнения четыре электрона:
С + 2Н2О - 4е ® СO2 + 4Н+
Окислителем служит ион NO3- , превращающийся в NO, Баланс масс обеспечивается в этом случае добавлением двух молекул H2O в правую часть уравнения и четырех ионов Н+ в его левую часть. Поскольку суммарный заряд частиц в левой части уравнения равен плюс три, а в правой - нулю, к левой части необходимо добавить три электрона:
NO3- + 4Н+ + 3е ® NO + H2O
3. Суммируют уравнения полуреакций, предварительно уравняв числа отданных и принятых электронов:
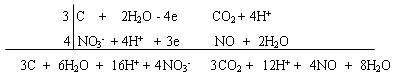
После сокращения подобных членов, получают ионное уравнение:
ЗС + 4H+ + 4NO3- ® ЗСО2 + 4NO + 2Н2О
4. Объединяют ионы в молекулы и получают итоговое молекулярное уравнение реакции:
3С + 4НNO3 ® 3СО2 + 4NO + 2Н2О
Сравнивая рассмотренные метода составления уравнений окислительно-восстановительных реакций, следует отметить, что оба они приводят к одинаковому конечному результату. Однако метод электронно-ионных уравнений более информативен, он оперирует не гипотетическими, а реальными ионами и молекулами, существующими в растворах электролитов. Особенно полезен он при описании электрохимических процессов.
5.2. Электрохимические системы.
Электродные потенциалы. Электрохимическими называются процессы взаимного превращения химической и электрической энергии. Эти превращения осуществляются в результате окислительно-восстановительных реакций, протекающих на границе раздела фаз между электронным и ионным проводниками. Электронный проводник, находящийся в контакте с ионным, называется электродом.
Рассмотрим электрод, состоящий из пластинки активного металла - цинка, погруженной в водный раствор сульфата цинка, диссоциирующего на ионы:
ZnSO4 ↔ Zn2+ SO42-
Положительно заряженные катионы цинка, расположенные на поверхности пластинки, в результате взаимодействия с полярными молекулами воды отрываются от пластинки и переходят в раствор, электроны остаются в металле. Происходит процесс окисления:
Zn 0 – 2е ® Zn2+
Одновременно протекает и обратный процесс: катионы цинка из раствора притягиваются поверхностью металла и входят в состав его кристаллической решетки. Идет процесс восстановления:
Zn2++2е ® Zn 0
По мере увеличения концентрации катионов цинка в растворе скорость выхода ионов из металла уменьшается, а скорость их перехода в металл возрастает. Когда скорости этих процессов сравняются, на границе металл-электролит установится окислительно-восстановительное равновесие между металлом и его ионами, которое условились записывать как обратимый процесс восстановления:
![]()
При записи электрохимической схемы электрода его окисленную форму отделяют от восстановленной чертой: Zn+2/Zn.
Поскольку цинк является активным металлом, равновесие процесса смещено влево, то есть в раствор переходит больше ионов, чем возвращается обратно. В результате цинковая пластинка приобретает отрицательный потенциал (рис. 5.1 а).
Те же процессы происходят и при погружении пластинки из малоактивного металла- меди в раствор сульфата меди, диссоциирующего на ионы:
CuSO4 ↔ Cu2+ + SO42-
Однако в этом случае металл посылает в раствор незначительное число катионов, преобладает процесс осаждения катионов на металле и равновесие смещено вправо:
![]()
Медный электрод Сu2+/Сu приобретает положительный потенциал (рис. 5.1.).

Рисунок 5.1. Схема возникновения электродного потенциала
а) активного металла; б) малоактивного металла
Абсолютную величину электродного потенциала измерить невозможно, поэтому измеряют ее относительно потенциала электрода сравнения, в качестве которого используют стандартный водородный электрод (рис.5.2). Он представляет собой платиновую пластинку в водном растворе серной кислоты с концентрацией ионов водорода Сн+ = 1 моль/л, омываемую водородом с давлением 101,3 кПа при температуре 293К.
Платина обладает способностью адсорбировать водород и на границе

Рисунок 5.2. Схема водородного электрода
раздела фаз устанавливается равновесие между молекулами и ионами водорода:
![]() 2Н + +
2е ↔ Н2
2Н + +
2е ↔ Н2
Соответствующий электродный потенциал условно принимают за нуль, Е0 2Н+/ Н2 = 0.
Стандартным электродным потенциалом металла называют разность потенциалов между данным металлом, опущенным в раствор своей соли с концентрацией ионов металла СМn+ =1 моль/л при температуре 293К и стандартным водородным электродом.
Стандартный электродный потенциал является мерой окислительно-восстановительной активности системы.
С увеличением величины стандартного электродного потенциала восстановительная активность системы уменьшается, а окислительная - растет.
Так, с ростом величины стандартного электродного потенциала металлов уменьшается восстановительная активность их атомов и растет окислительная активность ионов.
Сравнение электродных потенциалов полуреакций позволяет сделать вывод о направлении окислительно-восстановительного процесса.
Рассмотрим гетерогенную окислительно-восстановительную реакцию, протекающую при погружении цинковой пластинки в раствор сульфата меди, диссоциирующего на ионы (рис. 5.3а):
CuSO4 ↔ Cu2+ + SO42-
Электродные потенциалы цинка и меди имеют следующие значения:
Zn2+ + 2е ↔ Zn0; E0 = - 0,76B
Cu2+ + 2e ↔ Cu0; E0 = +0,34B
Как видно, стандартный электродный потенциал для второй системы выше, чем для первой. Следовательно, при контакте вторая система выступит в качестве окислителя, первая - в качестве восстановителя. Другими словами, вторая реакция пойдет слева направо, а первая - в противоположном направлении, то естъ цинк будет отдавать электроны ионам меди, вытесняя, таким образом, медь из раствора ее соли (рис. 5.3 а):
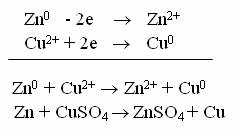
Электродный потенциал возникает не только в результате обмена ионами между металлом и раствором его соли. Любая окислительно-восстановительная полуреакция характеризуется определенным значением электродного потенциала, например:
СО2 + 4Н+ + 4е ↔ С + 2Н2О; Е° = +0,21B ,
NO3- + 4Н+ + 3e ↔ NO + 2H2; E° = +0,96B
В этом случае окислительные свойства сильнее выражены у иона NO3-, поэтому этот ион будет окислять углерод, восстанавливаясь до оксида азота NO (см.5.1).
Величина электродного потенциала не является постоянной, она зависит от ряда факторов, в частности от соотношения окисленной и восстановленной форм вещества. Эта зависимость выражается уравнением Нернста, которое при стандартной температуре 293К записывается в виде:
(5.1),
где: Е - электродный потенциал при данных концентрациях окисленной Сок и восстановленной Свосст форм вещества, моль/л,
Е° - стандартный электродный потенциал,
n - число переданных электронов.
Для металлических электродов в растворах солей восстановленной формой являются атомы металла, концентрация которых - величина постоянная СM = const. В этом случае уравнение Нернста приобретает вид:
(5.2)
где:
См+n - концентрация ионов металла, моль/л;
n - заряд иона.
Химические источники электрического тока. В рассмотренных системах переход электронов от восстановителя к окислителю осуществляется хаотически, в результате химическая энергия превращается в тепловую.
Можно, однако, пространственно разделив процессы окисления и восстановления, получить направленное движение электронов - электрический ток. Устройство, в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую, называется химическим источником тока или гальваническим элементом.

Рисунок 5.3. Гетерогенный окислительно-восстановительный процесс:
а – пространственно неразделенный; в – пространственно разделенный
На рис.5.3 изображена схема гальванического элемента Даниэля - Якоби, состоящего из цинкового и медного электродов, помещенных в водные растворы сульфатов этих металлов. Растворы соединены электролитическим мостиком — трубкой, заполненной раствором электролита, например, хлорида калия. При замыкании электродов через нагрузку на цинковом электроде идет процесс окисления с выходом ионов Zn2+ раствор; освободившиеся электроны переходят по внешней цепи на медный электрод, где восстанавливают ионы Сu+2 поступающие из раствора сульфата меди.
Электрод, на котором идет процесс окисления, называется анодом, электрод, на котором протекает процесс восстановления, - катодом. В медно-цинковом элементе цинковый электрод является анодом, медный - катодом. В процессе работы элемента цинковый анод постепенно растворяется, на медном катоде осаждается медь. Таким образом, цинковый электрод является активным, его материал принимает непосредственное участие в окислительно-восстановительном процессе. Медный электрод играет пассивную роль проводника электронов, его материал в окислительно-восстановительном процессе не участвует.
Окислительно-восстановительный процесс, протекающий на электродах, нарушает ионное равновесие в растворах - у медного электрода образуется избыток ионов SO42-, у цинкового - их недостаток. В результате во внутренней цепи возникает движение ионов SO42- из раствора сульфата меди в раствор сульфата цинка.
Электрохимическая схема этого элемента может быть записана в виде:

где одна вертикальная черта означает границу между электронным и ионным проводниками, а две - границу между двумя ионными проводниками.
Электродвижущая сила (ЭДС) элемента при стандартных концентрациях ионов (1 моль/л) может быть вычислена как разность стандартных потенциалов катода и анода:
ЭДС = DЕ° = Е0кат - Е 0ан = Е0 Сu2+/ Сu - Е0 Zn2+/ Zn = +0,34 - (- 0,76) = 1,1B.
Если концентрации ионов отличаются от стандартных, необходимо по формуле 5.2 вычислить потенциалы электродов при заданных концентрациях и затем взять их разность.
В принципе любая окислительно-восстановительная реакция может быть использована для получения электрической энергии при условии пространственного разделения процессов окисления и восстановления. Активными материалами электродов могут быть не только металлы, но и неметаллы, а также оксиды, гидроксиды и другие сложные вещества. Так, в случае реакции окисления углерода азотной кислотой (см. 5.1) электрический ток может быть получен, если в раствор азотной кислоты погрузить угольный и платиновый электроды и замкнуть их металлическим проводником. При этом активный угольный анод окисляется с образованием диоксида углерода СO2,на пассивном платиновом катоде идет восстановление нитрат-ионов NO3-до оксида азота NO. Схема элемента может быть записана в виде:
![]()
ЭДС =D Е° = Е°кат - Е°ан = Е°NO3-/ NO - E°CO2/ C = 0,96 - 0,21 = 0,75В
Величина DЕ° связана со стандартной энергией Гиббса реакции (DG°) соотношением:
DG°=-nFDE° (5.3)
где n- число переданных в ходе реакции электронов, F - число Фарадея (96500Кл).
Уравнение 5.3 устанавливает связь между химической и электрической формами энергии. Оно позволяет по известному значению G рассчитать Е гальванического элемента и наоборот, зная Е рассчитать G .
Топливные элементы. Топливный элемент является разновидностью гальванического элемента, в котором электрическая энергия получается в результате окислительно-восстановительного процесса между компонентами топлива - горючим (восстановителем) и окислителем, непрерывно подводимыми к электродам извне. Горючим может служить водород, моноксид углерода, метан, спирты, а окислителем - кислород, воздух, пероксид водорода и другие вещества. Таким образом, в топливных элементах, в отличие от тепловых машин, химическая энергия топлива непосредственно превращается в электрическую, поэтому их КПД в 1,5 - 2,0 выше, чем у тепловых машин. Кроме того, они существенно меньше загрязняют окружающую среду.

Рисунок 5.4. Водородно-кислородный топливный элемент
В настоящее время практическое применение нашел водородно-кислородный топливный элемент (рис.5.4).
Он содержит два пористых металлических или угольных электрода с добавками катализатора. В качестве электролита используется водный 40 - 85% раствор гидроксида калия. Электрохимическая схема элемента:
![]()
Подаваемые к электродам газообразные водород и кислород диффундируют через электроды в направлении электролита, адсорбируются на поверхности пор и активируются катализатором. Это облегчает и ускоряет процессы окисления водорода на аноде и восстановление кислорода на катоде:
H2 + 2OH- - 2е ® 2H2O
1/2О2 + Н2О + 2е ® 2ОН-
Суммарное уравнение реакции:
Н2+1/2О2 ® Н2О
Продукт реакции - парообразная вода отводится потоком водорода, который после отделения воды возвращается обратно в систему. Таким образом, осуществляется «холодное сжигание» водорода в кислороде с выделением энергии в электрической форме.
Аккумуляторы. Окислительно-восстановительные процессы, протекающие при работе гальванических элементов, могут иметь либо необратимый, либо обратимый характер. Соответственно химические источники тока могут быть однократного и многократного действия. Гальванические элементы многократного действия называются аккумуляторами. При работе аккумулятора в режиме источника тока самопроизвольно протекает окислительно-восстановительный процесс, приводящий к превращению химической энергии в электрическую (энергия Гиббса реакции отрицательна DG<0). Химический состав электродов при этом меняется, аккумулятор разряжается. Обратная реакция самопроизвольно не идет (DG>0). Однако разряженный аккумулятор можно зарядить от внешнего источника тока, напряжение которого превышает ЭДС элемента. При этом идет обратный процесс превращения электрической энергии в химическую и материал электродов регенерируется.
Окислительно-восстановительный процесс, протекающий при пропускании тока через электролит, называется электролизом.
В результате электролиза аккумулятор может вновь работать как источник тока. Число циклов заряд - разряд может достигать несколько сотен. В авиации находят применение свинцовый, серебряно-цинковый и кадмий-никелевый аккумуляторы.
Свинцовый (кислотный) аккумулятор в заряженном состоянии отвечает электрохимической схеме:
![]()
В режиме источника тока при разряде на отрицательном электроде происходит окисление свинца, а на положительном — восстановление диоксида свинца. При заряде идут обратные процессы: на отрицательном электроде - восстановление сульфата свинца, на положительном - его окисление:

В заряженном свинцовом аккумуляторе, в зависимости от его типа, концентрация серной кислоты составляет 27 - 30% масс. При разряде она cнижается, так как в электролит выделяется вода. Плотность электролита при этом также уменьшается. Это дает возможность, измеряя плотность электролита, контролировать степень разряда аккумулятора.
Кадмий-никелевый аккумулятор выполнен по схеме:
![]()
При разряде на отрицательном электроде Cd окисляется, на положительном - Ni(OH)3 частично восстанавливается. При заряде идут обратные процессы:

Кадмий-никелевые аккумуляторы стабильны в работе, требуют меньше ухода и отличаются большим сроком службы, чем свинцовые.
Серебряно-цинковый аккумулятор в заряженном состоянии соответствует схеме:
![]()
При его работе протекают обратимые реакции: на отрицательном электроде - окисление цинка, на положительном - восстановление оксида серебра:

Главным преимуществом серебряно-цинкового аккумулятора является его высокая энергоемкость; на единицу массы он дает в 4 - 6 раз больше энергии, чем рассмотренные типы аккумуляторов.
Коррозия металлов. Коррозия – это разрушение металла в результате его физико-химического взаимодействия с окружающей средой. Наиболее опасным и наиболее распространенным видом коррозии металлов является электрохимическая коррозия, которая происходит при контакте металлов с растворами электролитов. Чаще всего она является следствием работы короткозамкнутых гальванических элементов, которые образуются, например, при контакте деталей из разнородных металлов.
Роль электролита в этом случае может выполнять тонкая пленка влаги, образующаяся при адсорбции на металлических поверхностях водяного пара из атмосферы. Так, при контакте деталей из меди и железа в присутствии воды образуется гальванический элемент (рис.5.5):

Рисунок 5.5. Схема электрохимической коррозии
![]()
Железо, как более активный металл, служит анодом и подвергается окислению, на медном же катоде восстанавливается с участие воды кислород воздуха:

Для защиты металлов от коррозии используют различные покрытия: металлические, неметаллические, лакокрасочные, полимерные.
Примерные вопросы для самооценки:
1. Какие реакции называют окислительно-восстановительными?
2. Что понимают под восстановителем, окислителем?
3. В чем смысл метода электронных уравнений?
4. В чем смысл метода электронно-ионных уравнений?
5. Какие процессы называют электрохимическими?
6. Что такое стандартный водородный электрод?
7. Что является мерой окислительно-восстановительной активности системы?
8. Какую зависимость выражает уравнение Нерста?
9. Что называется гальваническим элементом?
10. Что называется катодом, анодом?
11. Как протекают окислительно-восстановительные процессы в аккумуляторах?
12. Что такое электролиз?
13. Что такое электрохимическая коррозия?
Задачи к теме № 5
Задача № 5.1.
Методом электронного баланса составить уравнения окислительно-восстановительных реакций. Указать окислитель и восстановитель:
1. NH3+O2 NO+H2O
2. HClO3 ClO2 + HClO4+H2O
3. AgNO3 Ag+NO2+O2
4. NH4 NO2+H2O
5. H2O2+PbS PbSO4+H2O
6. (NH4)2Cr2O7 N2+Cr2O3+H2O
7. Ca3(PO4)2+C+SiO2 CaSiO3+P+CO
8.
9. N2H2+O2 N2+H2O
10. S+KOH K2SO3+K2S+H2O
Задача № 5.2.
Составить уравнения окислительно-восстановительных реакций:
1) методом электронного баланса;
2) ионно-электронным методом.
Указать окислитель и восстановитель.
1. P+NO3 H3PO4+NO2+H2O
2. Zn+HNO3 Zn(NO3)2 NO2+H2O
3. K2Cr2O7+H2S+H2SO4 S+Cr2(SO4)3+K2SO4+H2O
4. KMnO4+KNO2+H2O KNO3+MnO2+KOH
5. FeSO4+H2O2+H2SO4 Fe2(SO4)3+H2O
6. CrCl3+H2O2+NaOH Na2CrO4+NaCl+H2O
7. CrO3+KNO3+KOH K2CrO4+KNO2+H2O
8. PH3+KMnO4+H2SO4 H3PO4+K2SO4+MnSO4+H2O
9. Si+NaOH+H2O Na2SiO3+H2
10. HCl+KMnO4 Ci2+MnCl2+KCl+H2O
Задача № 5.3.
Рассчитать электродный потенциал железа, погруженного в 0,05 молярный раствор Fe2(SO4)3. Диссоциацию считать полной.
Решение:
Электродный потенциал рассчитывается по формуле Нернста, которая для металлических и водородного электродов записывается в виде:
,
где Е – электродный потенциал,
n – заряд иона металла (водорода).
Уравнение диссоциации сульфата железа:
Fe2SO4 2Fe3++3SO42-
показывает, что при диссоциации 0,05 моль Fe2(SO4)3 образуется 0,05 2=0,1 моль ионов Fe3+ .
Следовательно С(Fe3+)=0,1 моль/л, n=3.
Из таблицы 3 имеем E0(Fe3+/Fe)=-0,04.
Задача № 5.4.
Рассчитать электродный потенциал хрома, погруженного в 0,01 молярный раствор Cr2(SO4)3.
Задача № 5.5.
На сколько изменится потенциал цинкового электрода, если раствор соли цинка, в который он погружен разбавить в 10 раз.
Задача № 5.6.
Потенциал кадмиевого электрода в растворе его соли равен 0,52В. Рассчитать концентрацию ионов Сd+ в растворе.
Задача № 5.7.
Рассчитать потенциал водородного электрода, погруженного в раствор с рН=3. (см. таблицу 3).
Задача № 5.8.
Вычислить рН раствора, в котором потенциал водородного электрода равен – 100 mB.
Задача № 5.9.
Рассчитать потенциал окислительно-восстановительного электрода при заданных значениях концентрации ионов и рН.
|
№ |
Уравнение реакции |
Концентрация ионов, С моль/л |
рН |
|
1 |
MnO4-+8H++5e Mn2++4H2O |
C(MnO4-)=C(Mn2+)=1 |
5 |
|
2 |
ClO3-+6H++6e Cl-+3H2O |
C(ClO3-)=C(Cl-)=0,1 |
6 |
|
3 |
Cr2O72-+14H++6e 2Cr3++7H2O |
C(Cr2O72-)=C(Cr3+)=1 |
3 |
|
4 |
PbO2+4H++2e Pb2++2H2O |
C(Pb2+)=0,1 |
4 |
Решение 1:
Потенциал окислительно-восстановительного электрода Е рассчитывают по уравнению Нерста:
,
где Е0 стандартный электродный потенциал;
n – число участвующих в реакции электронов;
Сок, Свосст – произведения концентраций веществ, находящихся в окисленной и восстановленной формах соответственно.
В данной системе в окисленной форме находятся ионы Mn4- и H+, в восстановленной – ион Mn2+ и молекула Н2О. В реакции принимает участие 5 электронов. Учитывая, что концентрация воды практически остается постоянной и входит в значение Е0, имеем:
По данным таблицы 3: Е0(MnO4-/Mn2+)=+1,51В.
Подставляя числовые значения получим окончательно:
Задача № 5.10.
Написать уравнения электродных процессов, протекающих при работе гальванического элекмента. Вычислить ЭДС элемента при заданных концентрациях, С моль/л.
|
№ |
Схема элемента |
С, моль/л |
|
1 |
Zn/Zn2+//Pb2+/Pb |
C(Zn2+)=0,2, C(Pb2+)=0,04 |
|
2 |
Mn/Mn2+//Ni2+/Ni |
C(Mn2+)=0,1, C(Ni2+)=0,01 |
|
3 |
Fe/Fe2+//Cu2+/Cu |
C(Fe2+)=1, C(Cu2+)=0,5 |
|
4 |
H2/2H+//Ag+/Ag |
C(H+)=0,01, C(Ag+)=0,1 |
|
5 |
Ni/Ni2+(C1)//Ni2+(C2)/Ni |
C1(Ni2+)=0,1, C2(Ni2+)=0,01 |
|
6 |
Cu/Cu2+//Fe3+/Fe2+ |
C(Cu2+)=1, C(Fe3+)=C(Fe2+)=1 |
Решение 1:
На основании данных таблицы 3 можно заключить, что более активный металл цинк будет в данном элементе анодом, а менее активный металл свинец – катодом.
Уравнения электродных процессов:

ЭДС гальванического элемента равна разности электродных потенциалов окислителя (катода) и восстановителя (анода):
Используя формулу Нерста, имеем:
Задача № 5.11.
Установить, в каком направлении возможно самопроизвольное протекание в стандартных условиях данной реакции. Рассчитайте величину константы равновесия реакции.
|
№ |
Уравнение реакции |
|
1 |
2Сl-+2Fe3+ 2Fe2++Cl2 |
|
2 |
H2O2+HClO H+Cl+O2+H2O |
|
3 |
5H2O2+H++2IO3 I2+5O2+6H2O |
|
4 |
Sn4++2I- Sn2++I2 |
|
5 |
Sn4++H2S Sn2++S+2H+ |
|
6 |
H2S+4H2O2 2H++SO42-+4H2O |
Решение 1:
Для определения направления окислительно-восстановительной реакциинеобходимо найти ЭДС гальванического элемента, образованного из дпнного окислителя и восстановителя.
,
где Е0ок, Е0восст – стандартные потенциалы окислителя и восстановителя.
Возможна та реакция, для которой , так как в этом случае изменение энергии Гиббса – отрицательная величина.
,
где n- число участвующих в реакции электронов;
F – число Фарадея, равное 96480 Кл/моль.
В свою очередь, изменение энергии Гиббса связано с константой равновесия соотношением:
Следовательно,
,
откуда
, .
Стандартные электродные потенциалы равны (см. таблицу 3):
Cl2+ 2e 2Cl- E0(Cl2/2Cl-)=1,36 B
Fe3+ + e Fe2+ E0(Fe3+/Fe2+=0,77 B
Поскольку Е0 (Сl2/2Сl)>E0(Fe3+/Fe2+) окислителем будет служить хлор, а восстановителем – ион Fe2+.
Уравнения электродных процессов:

Суммарное уравнение:
Cl2+2Fe2+ 2Cl- + Fe3+
Таким образом, рассматриваемая реакция будет протекать справа налево.
К=1020
Задача №5.12.
Рассчитать величину потенциала окислительно-восстановительного электрода, полученного при погружении платиновой проволоки в водный раствор, содержащий одновременно две соли А и В с концентрациями СА и СВ, моль/л при заданном значении водородного показателя рН.
|
№ |
А |
В |
СА |
СВ |
рН |
|
1 |
Na2Cr2O7 |
Cr2(SO4)3 |
0,1 |
0,2 |
4 |
|
2 |
NaClO2 |
NaClO |
0,1 |
0,3 |
9 |
|
3 |
KClO4 |
NaClO3 |
0,2 |
0,3 |
3 |
|
4 |
Na2SO4 |
K2SO3 |
0,05 |
0,08 |
10 |
|
5 |
CrCl3 |
CrCl2 |
0,2 |
0,8 |
1 |
|
6 |
NaNO3 |
NaNO2 |
0,01 |
0,09 |
9 |
|
7 |
Na2S2O8 |
Na2SO4 |
0,1 |
0,2 |
6 |
|
8 |
KMnO4 |
K2MnO4 |
0,3 |
0,6 |
8 |
|
9 |
Fe2(SO4)3 |
FeSO4 |
1 |
3 |
2 |
|
10 |
Ce(SO4)2 |
Ce2(SO4)3 |
0,002 |
0,001 |
0,5 |
Решение 1:
Раствор, содержащий одновременно окисленную и восстановленную форму одного и того же элемента (в данном случае, хрома), называется окислительно-восстановительной системой. В общем виде уравнение окислительно-восстановительной реакции для окислительно-восстановительного электрода имеет вид:
Ох+ne Red,
где n – число электронов, участвующих в реакции, а Ох и Red – окисленная и восстановленная форма элемента. Для определения величины электродного потенциала такой системы следует воспользоваться уравнением Нерста:
Формально в данном случае степень окисления в электродном процессе изменяет хром
Cr6+ + 3e Cr3+,
то есть окисленной формой будет Cr6+ - содержащая форма, однако это не означает, что можно записать по логарифмом в уравнении Нерста величину активности Cr6+. Это связано с тем, что сама по себе частица Сr6+ в водном растворе не существует, она входит в состав более сложной частицы Cr2O72-, поэтому понятие активности, то есть кажущейся концентрации несуществующих частиц Cr6+ лишено смысла. Можно определить активность (или концентрацию) частиц Cr2O72-, но тогда и уравнение электродного процесса следует записать с участием частиц Cr2O72-
Cr2O72- +…. Cr3+ +…,
однако в этом случае в левой части присутствует кислород, а в правой его нет, поэтому необходимо дописать в правую часть частицы, содержащие О2-. Ионов О2- в водном растворе нет, однако кислород с такой степенью окисления входит в состав либо молекул Н2О, либо ионов ОН-. Поскольку по условию среда является кислой (рН<7), концентрация ионов ОН- в этом растворе крайне мала, значит следует записывать электродный процесс на с участием этих ионов, а с участием молекул Н2О
Cr2O72- + 14Н+ + 6е 2Сr3+ + 7H2O
Таким образом, в электродном процессе помимо ионов Cr2O72- и Сr3+ участвуют и ионы Н+, поэтому их концентрация также будет влиять на величину электродного потенциала, то есть
По условию, концентрации К2Cr2O7 и Cr2(SO4)3 составляют соответственно 0,1 и 0,2 моль/л. Поскольку эти соли являются сильными электролитами, то есть диссоциируют в растворе нацело, концентрация ионов Cr2O72- и Cr3+ составят 0,1 и 0,4 моль/л. При рН=2 концентрация ионов Н+ равна С(Н+)=10-рН=10-2 , отсюда:
Ключевые понятия:
· реакция окисления;
· реакция восстановления;
· окислитель;
· восстановитель;
· уравнение окислительно-восстановительной реакции;
· электрохимическая система;
· стандартный водородный электрод;
· стандартный электродный потенциал;
· химический источник тока;
· катод;
· анод;
· топливный элемент;
· аккумулятор;
· электролиз;
· коррозия.